Study on the Performance of Nebulizer for Pressurized Intraperitoneal Aerosol Chemotherapy (PIPAC)
-
摘要:目的
对腹腔加压气溶胶化疗用雾化器进行性能研究。
方法通过激光衍射光谱法测量雾化器在稳态气溶胶阶段的中位粒径及喷雾角度。
结果当喷嘴直径为0.2 mm,喷嘴厚度为0.07 mm时,中位粒径最小;当液体流量小于等于0.3 mL/s时,无稳态气溶胶形成;当液体流量大于等于0.5 mL/s时,随着工作压力的增大,中位粒径逐渐减小,喷雾角度逐渐增大;当压力大于等于200 psi时,随着流量的增大,喷雾角度逐渐增大。当流量为0.7 mL/s,工作压力为300 psi时,气溶胶的中位粒径D50为16 μm,喷雾角度可达89.2°。
结论PIPAC作为一种新的腹腔内给药技术,在减少气溶胶的液滴尺寸,扩大空间药物分布、提高组织渗透和浓度方面还需进一步的研究。
Abstract:ObjectiveThe study aims to investigate the performance of an atomized drug feeder for pressurized intraperitoneal aerosol chemotherapy (PIPAC).
MethodsLaser diffraction spectroscopy was used to measure the median particle size and spray angle.
ResultsThe smaller droplet diameter of aerosol was achieved when using a nozzle diameter of 0.2 mm and a nozzle thickness of 0.07 mm. The nebulizer could not produce steady-state aerosol when the liquid flow rate was less than or equal to 0.3 mL/s. When the liquid flow rate is greater than or equal to 0.5 mL/s, as the working pressure increases, the median particle size gradually decreases and the spray angle gradually increases.When the pressure exceeded or equaled 200 psi,as the liquid flow rate increases, the spray angle gradually increases.At a flow rate of 0.7 mL/s and working pressure of 300 psi, the median droplet diameter of aerosol D50 was 16 μm with a corresponding spray angle up to 89.2°.
ConclusionAs a novel intraperitoneal drug delivery technology, PIPAC requires further research focusing on reducing droplet sizes , expanding drug distribution , as well as improving tissue penetration and concentration levels.
-
0. 引言
腹膜转移(peritoneal metastasis, PM)是多种原发性肿瘤的常见转移部位,均与预后不良相关。全身化疗是主要的治疗手段,但并发症发病率高,生存获益较少。细胞减灭术和腹腔热化疗对少部分患者是一种潜在治愈方法,但大部分患者最终会出现复发[1]。目前常见的治疗方法包括细胞减灭手术(cytoreductive surgery, CRS)、经导管腹腔化疗、腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy, HIPEC)等,但均没有提供一个令人满意的临床结果[2]。
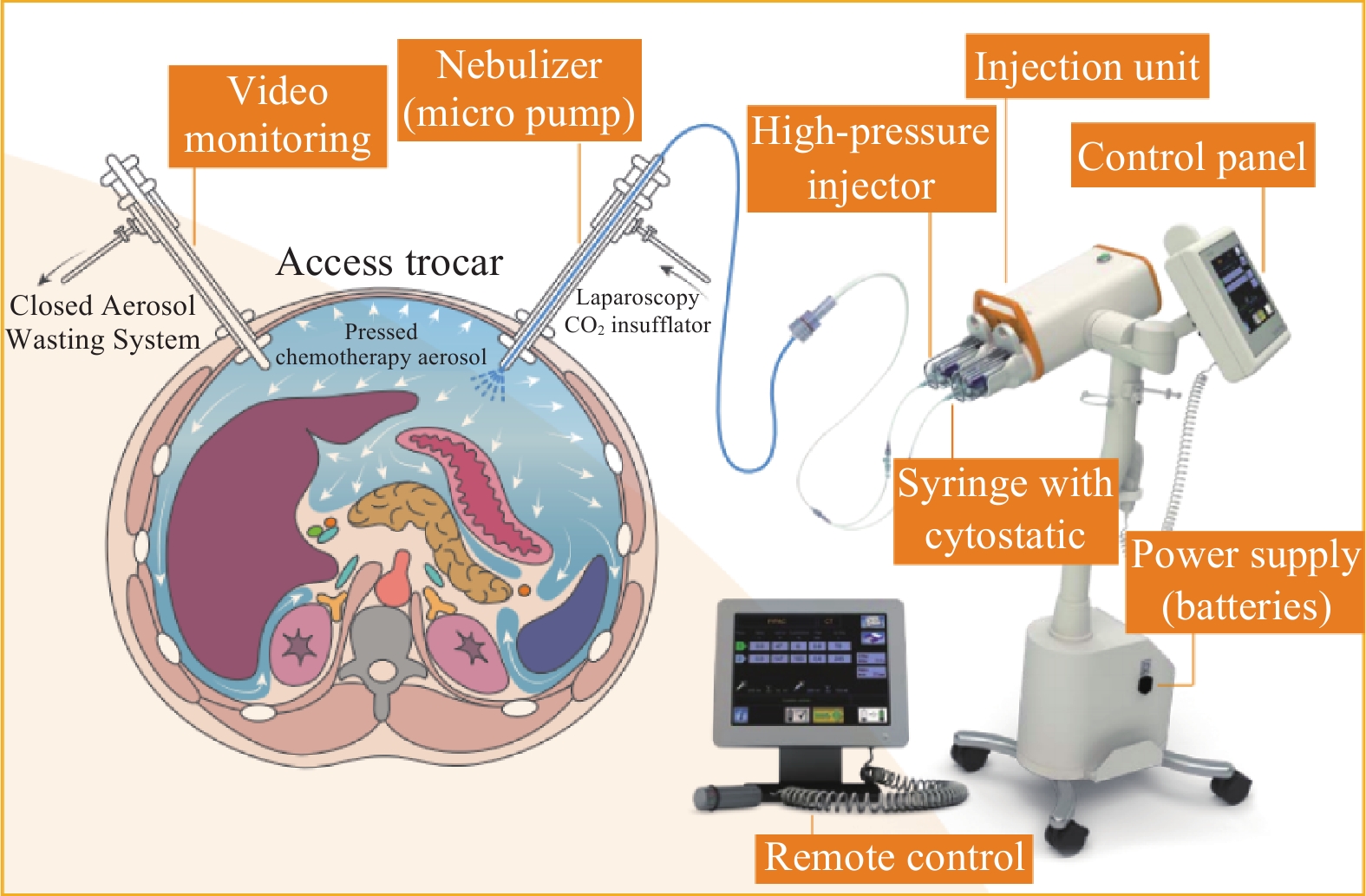
2011年,欧洲开发并引进了一种新的治疗方法腹腔加压气溶胶化疗(pressurized intraperitoneal aerosol chemotherapy, PIPAC),目前已在全球越来越多的医院中得到应用。该方法是一种新的腹腔内给药技术,通过将药物雾化成气溶胶加压后注入腹腔,气溶胶直接接触腹膜,以达到治疗的目的。该治疗方法的手术装置连接如图1所示。
图1中雾化器一端与高压注射器连接,一端通过穿刺器插入腹腔建立的通道进入腹腔,通过高压将药液压入雾化器,药液流经雾化器内部的机械结构后将液体雾化,雾化后的液体以气溶胶的形式从喷头喷出,分散到腹腔内,作用到病灶组织。气溶胶的中位粒径越小,越有利于药液扩散及组织的吸收;雾化角度越大,越有利于增大药物与病变组织表面的接触,增强治疗效果。
PIPAC 较其他腹腔给药方法有以下几个方面的优势:1气溶胶对化疗药的增强作用:与传统腹腔给药相比,PIPAC 中化疗药物通过加压雾化形成气溶胶喷洒在腹膜表面,增加肿瘤组织间液压力,从而提高药物穿透深度及分布浓度,药物的分布更均匀,可能导致药物更好地穿透深部腹膜癌组织,进而更好地控制腹膜肿瘤组织的增殖。与全身化疗相比,PIPAC在腹腔内可以产生较高的药物浓度,却具有最小的全身毒性。2腹腔加压对组织摄取率的增强作用:PIPAC 治疗中,腹腔内压力比其他腹腔给药方法腹腔内的压力更高,而压力梯度驱动力是决定腹腔肿瘤组织间药物吸收速度的重要因素之一,在一定的压力范围内,增加压力能够增强压力梯度驱动力,进而增加肿瘤组织对药物的摄取率[2]。
这种创新性技术经历了多次改进,临床前研究显示,PIPAC 能很好地使药物穿透肿瘤结节,并在腹腔均匀分布[3]。此后,建立了高度标准化的治疗模式,多个国际专家小组多次组织了结构化的培训会议,以便医护人员能够安全地实施 PIPAC[4]。在欧洲,PIPAC 已被广泛应用,目前正在进行几项大型临床试验,包括不同适应证的Ⅰ期、Ⅱ期和Ⅲ期试验,其中有代表性的是一项针对胃癌腹膜转移患者的Ⅱ期多中心临床试验:(PIPAC EstoK 01) [5] 和一项针对上消化道癌腹膜转移患者的Ⅲ期多中心临床试验[6],下一步是开展更多的试验来评估长期疗效和随访阶段。
本文主要对实现PIPAC疗法的雾化器从技术特征及工作原理、雾化性能等方面进行研究。
1. 材料和方法
1.1 试验材料及装置
雾化器由双九医疗科技(天津)有限公司生产,分析液体采用0.9%氯化钠溶液(注:由于临床常用0.9%氯化钠注射液配置化疗药物,故本文中的测试采用0.9%氯化钠溶液进行),激光衍射光谱法采用喷雾激光粒度仪(Bettersize 2000S,丹东百特仪器有限公司),测试地点为双九公司的精密实验室。
本文所有试验中产品的装夹位置:雾化器喷嘴的出口通过工装固定在垂直于可自由接触的红色激光光束边缘的5 mm距离内,激光光束直径为15 mm,喷头到激光发射口的轴向距离为20 mm,具体如图2所示。
1.2 喷嘴直径、喷嘴厚度对中位粒径的影响
根据Daniel Göhler等[7]对微量注射泵 (microinjection pump, MIP)产品的研究,液体流量大于25 mL/min时,产品可产生稳态气溶胶。本次将流量设置为0.7 mL/s,压力设定为300 psi,研究喷嘴直径、喷嘴厚度对中位粒径的影响。
1.3 不同液体流量下,达到设定压力的时间
为了表征不同液体流量下,气溶胶从起始阶段到高压注射器(注:高压注射器的功率为0.6kW)到达设定压力所需时间的变化,分别设置0.3 mL/s、0.5 mL/s、0.7 mL/s三种液体流量,记录到达高压注射器设定压力250 psi的时间,所有分析重复3次。
1.4 气溶胶中位粒径和喷雾角度分析
通过激光衍射光谱法在0.1~
2000 μm的尺寸范围内表征液体产生的气溶胶的粒径分布及气溶胶的喷雾角度。雾化器喷嘴的出口通过工装固定在垂直于可自由接触的红色激光光束边缘的5 mm距离内。为了表征雾化性能,所有分析都在稳态气溶胶形成时进行,测量值在稳态气溶胶形成后获取,使用垂直于喷嘴方向的相机拍摄喷雾状态,使用影像测量仪测量喷雾角度,所有分析重复3次。2. 结果
2.1 喷嘴处气溶胶的速度
假设液体不可压缩性,气溶胶液滴的出口速度V可以根据液体流速QL与喷嘴孔口最小横截面积AD的连续性之比确定:
$$ V_{{\mathrm{D}}} = \frac{{\mathrm{Q}}_{\mathrm{L}}}{{A}_{{\mathrm{D}}}} = \frac{4\times {Q}_{\mathrm{L}}}{\text{π}\times {{d}_{{\mathrm{D}}}}^{2}} $$ (1) 将雾化器的QL=0.7 mL/s的液体流速和0.2 mm喷嘴孔直径代入公式(1),计算出口速度VD为22.3 m/s。
2.2 喷嘴直径、喷嘴厚度对中位粒径的影响
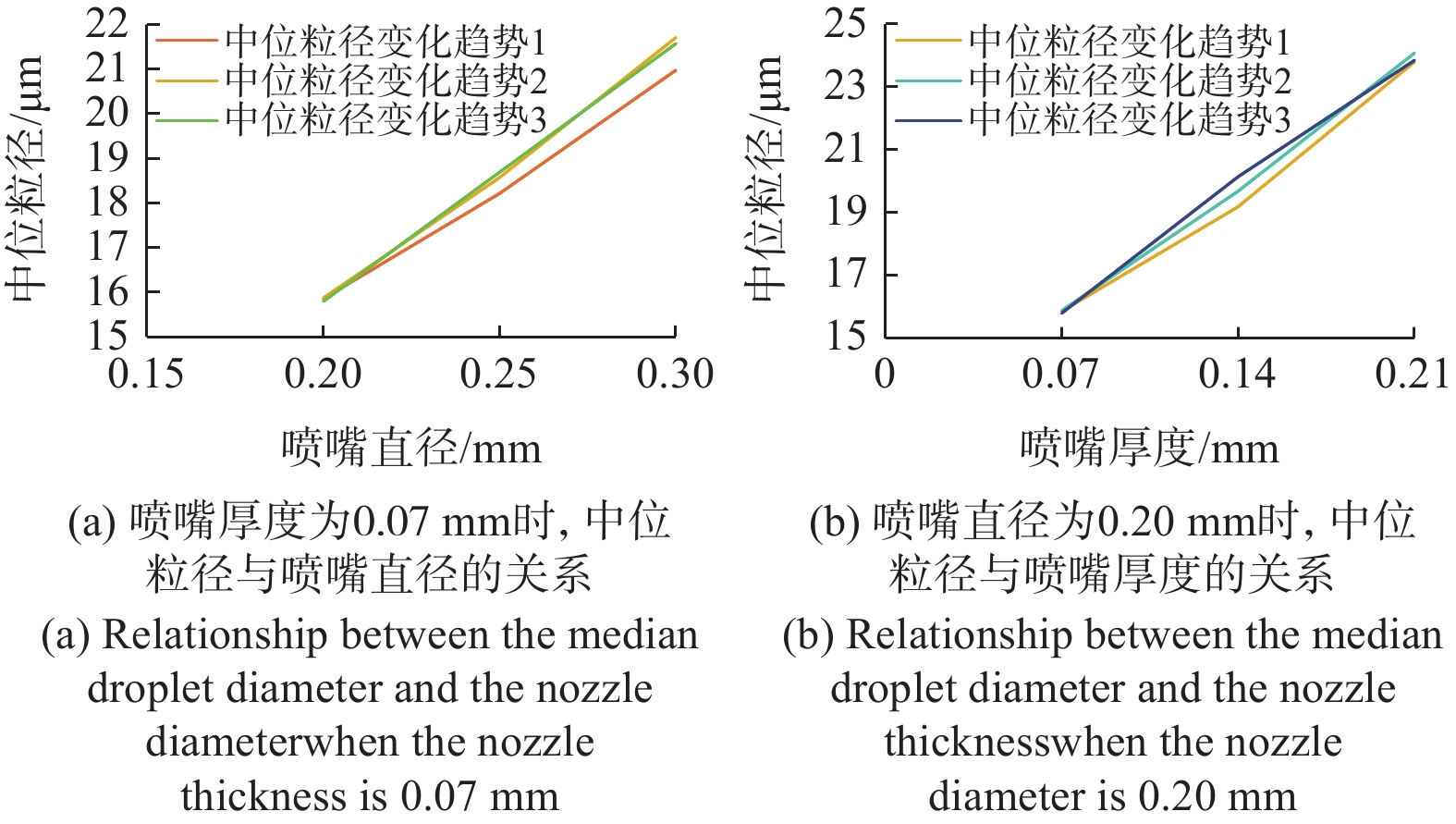
将高压注射器流量设置为0.7 mL/s,压力设定为300 psi,记录喷嘴直径分别为0.20 mm、0.25 mm、0.30 mm,喷嘴厚度为0.07 mm时,气溶胶中位粒径如表1所示;记录喷嘴厚度分别为0.07 mm、0.14 mm、0.21 mm,喷嘴直径为0.20 mm,气溶胶的中位粒径如表2所示。
表 1 喷嘴直径不同时,气溶胶的中位粒径D50Table 1. Median droplet diameterD50 of aerosol with different nozzle diameters单位: μm 喷嘴厚度/mm 喷嘴直径/mm 0.20 0.25 0.30 0.07 15.85 18.21 20.98 15.87 18.57 21.71 15.79 18.69 21.57 表 2 喷嘴厚度不同时,气溶胶的中位粒径D50Table 2. Median droplet diameter D50 of aerosol with different nozzle thickness单位: μm 喷嘴直径/mm 喷嘴厚度/mm 0.07 0.14 0.21 0.20 15.85 19.18 23.79 15.87 19.67 24.07 15.79 20.13 23.85 以上不同组合形式均在稳态气溶胶阶段测量,并重复3次。
图4给出了喷嘴厚度和喷嘴直径的变化对气溶胶中位粒径的影响。从3次测量的中位粒径变化曲线可知,当喷嘴厚度为0.07 mm时,随着喷嘴直径的增加,中位粒径呈逐渐增大的趋势;当喷嘴直径为0.2 mm时,随着喷嘴厚度的增加,中位粒径呈逐渐增大的趋势。当喷嘴直径为0.2 mm,喷嘴厚度为0.07 mm时,中位粒径最小,有利于气溶胶扩散及组织的吸收。
2.3 不同液体流量下,达到最大允许压力的时间
分别设定液体流量为0.3 mL/s、0.5 mL/s、0.7 mL/s,各测试3次,记录到达设定压力250 psi的平均时间如表3所示。
表 3 不同液体流量下,高压注射器到达设定压力的时间Table 3. Time when the high pressure syringe reaches the set pressure under different liquid flow流量/(mL/s) 3次测量的平均时间/s 0.3 该流量无法达到250 psi,未形成稳态气溶胶 0.5 69 0.7 57 当液体流量为0.3 mL/s时,高压注射器无法达到250 psi压力,雾化器无法喷出稳态气溶胶;当液体流量为0.5 mL/s时,高压注射器运行69 s后到达设定压力250 psi,雾化器可喷出稳态气溶胶;当液体流量为0.7 mL/s时,高压注射器运行57 s后到达设定压力250 psi,雾化器可喷出稳态气溶胶。
2.4 不同液体流量和工作压力下,气溶胶的粒径分布
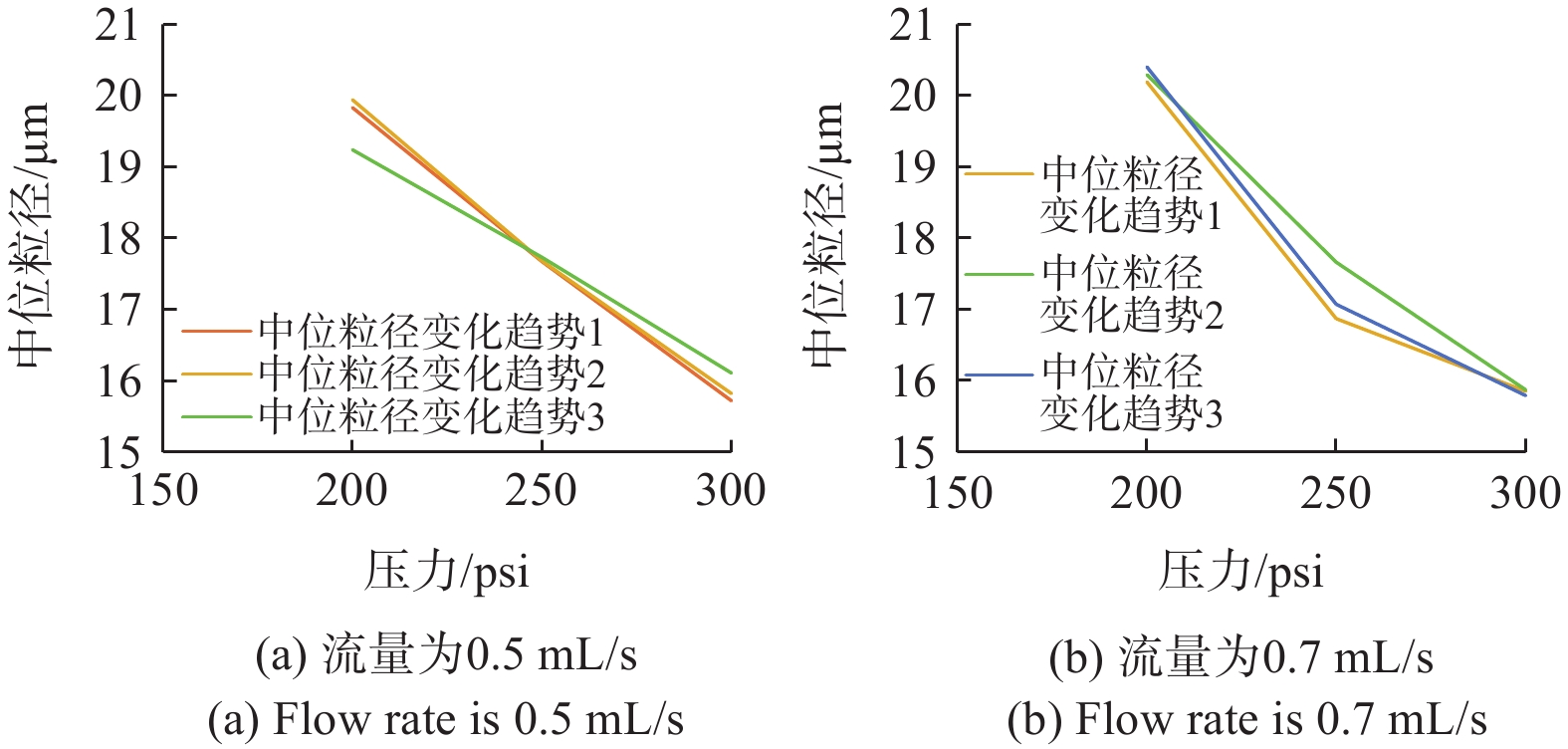
在压力分别为200 psi、250 psi和300 psi,液体流量分别为0.5 mL/s、0.7 mL/s时进行排列组合测试,均在稳态气溶胶阶段测试,并重复3次。记录每次测试的气溶胶的中位粒径D50,如表4所示。
表 4 不同流量和压力下,气溶胶的中位粒径D50Table 4. Median droplet diameter D50 at different flow rates and pressures单位: μm 流量/(mL/s) 压力/psi 200 250 300 0.50 19.83 17.67 15.72 19.94 17.68 15.82 19.24 17.73 16.11 0.70 20.19 16.87 15.85 20.29 17.66 15.87 20.40 17.07 15.79 图5给出了液体流量分别为0.5 mL/s和0.7 mL/s,压力分别为200 psi、250 psi、300 psi时气溶胶中位粒径的变化。从三次测量的中位粒径变化曲线可知,当流量一定时,随着压力的增大,中位粒径呈逐渐减小的趋势;当压力一定,气溶胶呈稳态喷出时,流量的变化对中位粒径的影响不明显。当压力为200 psi时,气溶胶的中位粒径为19~21 μm,国外临床应用的雾化器产品的中位粒径为21~30 μm[7];当压力为300 psi时,测试雾化器的气溶胶中位粒径为15~16 μm。气溶胶中位粒径越小,越有利于药物扩散及组织的吸收。
2.5 不同流量、不同压力下,喷雾角度的变化
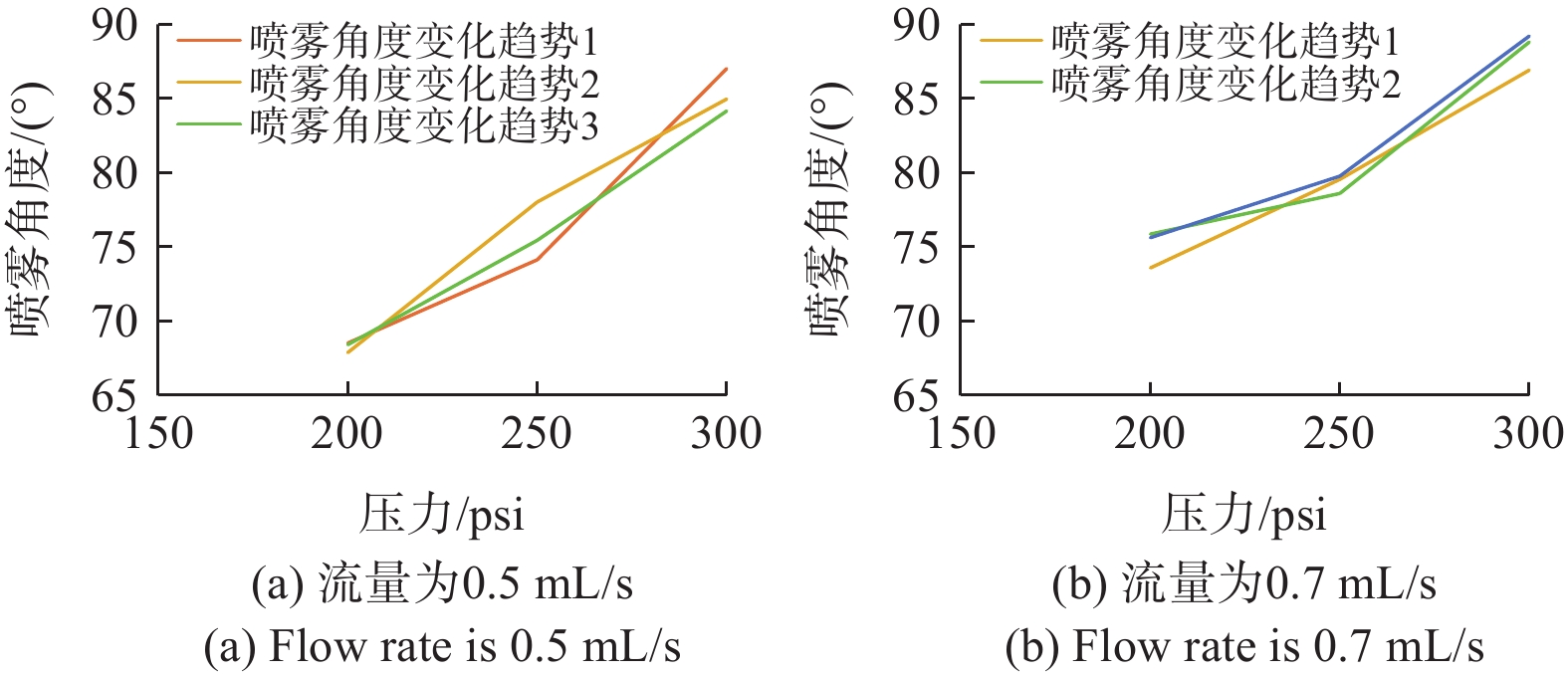
在压力分别为200 psi、250 psi和300 psi,流量分别为0.5 mL/s、0.7 mL/s时进行排列组合测试,均在稳态气溶胶阶段测试,并重复3次。记录每次测试的气溶胶的喷雾角度,如表5所示。
表 5 不同流量和压力下,气溶胶的喷雾角度Table 5. Aerosol spray Angle under different flow rate and pressure单位:° 流量/(mL/s) 压力/psi 200 250 300 0.50 68.52 74.13 87.01 67.89 78.03 84.96 68.42 75.45 84.16 0.70 73.59 79.55 86.91 75.87 78.60 88.8 75.62 79.77 89.21 图6及图7给出了气溶胶喷雾状态及不同流量及压力下,气溶胶喷雾角度的变化。从图7三次测量的喷雾角度的变化可知,当流量一定时,随着压力的增大,喷雾角度呈逐渐增大的趋势;当压力一定时,随着流量的增大,喷雾角度呈逐渐增大的趋势。流量为0.7 mL/s时,喷雾角度均大于70°;当流量为0.5 mL/s,压力为250 psi及以上时,喷雾角度均大于70°。
2.6 雾化器气溶胶粒度分布
根据上述多次测量结果,将流量设定为0.7 mL/s,压力设定为300 psi时,测试雾化器气溶胶的中位粒径小于16 μm,获取喷雾激光粒度仪上的典型粒度分布表,如表6所示。
表 6 典型粒度分布表Table 6. Typical particle size distribution粒径/μm 含量(%) ≤5 0.08 ≤15 45.12 ≤20 67.32 ≤30 90.10 ≤50 99.76 ≤100 100 从表6的数据可知,99.68 % 的液体以直径大于等于5 μm并且小于等于50 μm的气溶胶形式输送。
3. 讨论
本研究中雾化器有一个液体经过其内部机械结构后雾化成气溶胶的单流体喷嘴。分析了喷嘴直径和喷嘴厚度的变化对气溶胶中位粒径的影响,雾化器在不同流量时达到设定压力的时间及雾化器在不同流量、不同压力下的气溶胶特性。
当喷嘴厚度为0.07 mm时,随着喷嘴直径的增加,中位粒径呈逐渐增大的趋势;当喷嘴直径为0.2 mm时,随着喷嘴厚度的增加,中位粒径呈逐渐增大的趋势。通过上述变化趋势可知,当喷嘴直径为0.2 mm,喷嘴厚度为0.07 mm时,中位粒径最小,有利于气溶胶扩散及组织的吸收。根据上述喷嘴厚度和喷嘴直径的变化对中位粒径大小的影响趋势,当喷嘴厚度和喷嘴直径继续降低时,可能会使中位粒径进一步降低,待进一步的研究。
当流量等于或小于0.3 mL/s时,无法观察到稳态的气溶胶形成,当流量大于或等于0.5 mL/s时,可以观察到稳态的气溶胶,这与Daniel Göhler等[7]对国外临床使用的微量注射泵产品的研究结论相同,即当体积流速等于或高于 25 mL/min 时,发现稳定的气溶胶形成。随着流量的增大,雾化器到达设定压力250 psi的时间缩短,并可以使液体以稳态气溶胶的形式从喷嘴喷出,符合专家建议的市场上用于PIPAC治疗的新喷雾器的特征之一为:注射压力在10~20 bar时,喷雾器应能产生液滴[8]。
当流量大于或等于0.5 mL/s时,随着压力的增大,中位粒径呈逐渐减小的趋势;当压力大于等于200 psi时,气溶胶呈稳态喷出后,流量的变化对中位粒径的影响不明显。Daniel Göhler, Dipl.-Ing等[9]对国外4种不同喷雾器进行对比研究,研究表明每个喷雾器的喷嘴产生的液滴气溶胶的中位粒径显著取决于操作压力,随着操作压力的增加,中位粒径减小。
当流量大于或等于0.5 mL/s时,随着压力的增大,喷雾角度呈逐渐增大的趋势;当压力大于等于200 psi时,随着流量的增大,喷雾角度亦呈逐渐增大的趋势。流量为0.7 mL/s时,喷雾角度均大于70°,且最大可达89.2°;当流量为0.5 mL/s,压力为250 psi及以上时,喷雾角度均大于70°。Pocard M[8]等定义了喷雾角度至少为70°的最低要求,这意味着喷雾角度对应于可实现的药物沉积面积,药物沉积面积越大,治疗效果越好。
当流量设定为0.7 mL/s,高压注射器的工作压力设定为300 psi时,液体从喷嘴以大约22.3 m/s的速度喷出,以气溶胶的形式扩散。气溶胶的中位粒径约为16 μm,99.68 % 的液体以直径大于等于5 μm并且小于等于50 μm 的形式输送。这与Daniel Göhler等[7]对MIP的研究结果接近,即体积分数为97.5%的供应液体基于直径为 x>3 μm 的液滴,而体积分数为2.5 %的液滴由液滴X<3 μm(细小部分)组成。MIP产品的气溶胶中位粒径为25 μm,Daniel Göhler, Dipl.-Ing等[9]对国外4种不同喷雾器对比研究的气溶胶的中位粒径为21~30 μm,而本文研究的雾化器产品的气溶胶中位粒径更小,为16 μm,更有利于药物的扩散及吸收。
4. 结论
PIPAC目前已逐步使用于临床,属于一种新型的腹腔给药技术,现有文献中以回顾性研究较多,前瞻性研究较少,对于化疗药物选择、机制研究、与全身化疗等方式联合或单独比较研究等需要进一步深入研究,也是未来发展的方向。德国在PIPAC领域的相关研究处于领先地位,瑞士的中心性最高,PIPAC领域的相关研究暂未见中国参与,这预示着今后可在国内开展PIPAC领域的相关研究。
手术中腹腔镜不能进入腹部是 PIPAC 的一个局限性。对于 PIPAC 来说,腹腔镜入路粘连、腹膜间隙闭塞(网膜饼或大结节)、腹腔脏器水肿、肠扩张或门静脉高压症/肝硬化的相对禁忌证都会影响手术的进行。手术能否进行在很大程度上取决于患者的选择和手术者的手术能力,在 CRS、腹膜切除术和 HIPEC后,与其他手术相比,腹腔镜无法进入腹部的比率更高。
PIPAC作为一种新的腹腔内给药技术在临床治疗腹膜转移具有一定的优势并取得了鼓舞人心的疗效,提高了患者的生存质量,但药物在整个腹腔中分布不均匀,从而导致治疗不足仍是该方法面临的问题。因此,减少气溶胶的液滴尺寸,扩大空间药物分布、提高组织渗透和浓度方面还需进一步的研究。
-
表 1 喷嘴直径不同时,气溶胶的中位粒径D50
Table 1 Median droplet diameterD50 of aerosol with different nozzle diameters
单位: μm 喷嘴厚度/mm 喷嘴直径/mm 0.20 0.25 0.30 0.07 15.85 18.21 20.98 15.87 18.57 21.71 15.79 18.69 21.57 表 2 喷嘴厚度不同时,气溶胶的中位粒径D50
Table 2 Median droplet diameter D50 of aerosol with different nozzle thickness
单位: μm 喷嘴直径/mm 喷嘴厚度/mm 0.07 0.14 0.21 0.20 15.85 19.18 23.79 15.87 19.67 24.07 15.79 20.13 23.85 表 3 不同液体流量下,高压注射器到达设定压力的时间
Table 3 Time when the high pressure syringe reaches the set pressure under different liquid flow
流量/(mL/s) 3次测量的平均时间/s 0.3 该流量无法达到250 psi,未形成稳态气溶胶 0.5 69 0.7 57 表 4 不同流量和压力下,气溶胶的中位粒径D50
Table 4 Median droplet diameter D50 at different flow rates and pressures
单位: μm 流量/(mL/s) 压力/psi 200 250 300 0.50 19.83 17.67 15.72 19.94 17.68 15.82 19.24 17.73 16.11 0.70 20.19 16.87 15.85 20.29 17.66 15.87 20.40 17.07 15.79 表 5 不同流量和压力下,气溶胶的喷雾角度
Table 5 Aerosol spray Angle under different flow rate and pressure
单位:° 流量/(mL/s) 压力/psi 200 250 300 0.50 68.52 74.13 87.01 67.89 78.03 84.96 68.42 75.45 84.16 0.70 73.59 79.55 86.91 75.87 78.60 88.8 75.62 79.77 89.21 表 6 典型粒度分布表
Table 6 Typical particle size distribution
粒径/μm 含量(%) ≤5 0.08 ≤15 45.12 ≤20 67.32 ≤30 90.10 ≤50 99.76 ≤100 100 -
[1] WINKLER CS, SANDHU J, PETTKE E, et al. Pressurized intraperitoneal aerosol chemotherapy, a palliative treatment approach for patients with peritoneal carcinomatosis: description of method and systematic review of literature[J]. Dis Colon Rectum, 2020, 63: 242-255. doi: 10.1097/DCR.0000000000001565
[2] 王宁, 于鹏杰. 腹腔加压气溶胶化疗在胃癌腹膜转移中的研究进展[J]. 中国肿瘤临床, 2021, 48(22): 1181-1186. [3] GRASS F, VUAGNIAUX A, TEIXEIRA-FARINHA H, et al. Systematic review of pressurized intraperitoneal aerosol chemotherapy for the treatment of advanced peritoneal carcinomatosis[J]. Br J Surg, 2017, 104(6): 669-678. doi: 10.1002/bjs.10521
[4] NOWACKI M, ALYAMI M, VILLENEUVE L, et al. Multicenter comprehensive methodological and technical analysis of 832 pressurized intraperitoneal aerosol chemotherapy (PIPAC) interventions performed in 349 patients for peritoneal carcinomatosis tre atment: an international survey study[J]. Eur J Surg Oncol, 2018, 44(7): 991-996. doi: 10.1016/j.ejso.2018.02.014
[5] EVENO C, JOUVIN I, POCARD M. PIPAC EstoK 01: pressurized intraperitoneal aerosol chemotherapy with cisplatin and doxorubicin (PIPAC C/D) in gastric peritoneal metastasis: a randomized and multicenter phase Ⅱ study[J]. Pleura Peritoneum, 2018, 3(2): 20180116.
[6] OLIVER GOETZE T, AL-BATRAN S E, PABST U, et al. Pressurized intraperitoneal aerosol chemotherapy (PIPAC) in combination with standard of care chemotherapy in primarily untreated chemo naïve upper giadenocarcinomas with peritoneal seeding-a phase Ⅱ/Ⅲ trial of the AIO/CAOGI/ACO[J]. Pleura Peritoneum, 2018, 3(2): 20180113.
[7] GÖHLER D, KHOSRAWIPOUR V, KHOSRAWIPOUR T, et al. Technical description of the micro injection pump (MIP®) and granulometric characterization of the aerosol applied for Pressurized IntraPeritoneal Aerosol Chemotherapy (PIPAC)[J]. Surg Endosc, 2017, 31(4): 1778-1784. doi: 10.1007/s00464-016-5174-5
[8] POCARD M, SO J B Y, HUCHON C, et al. PIPAC nebulizer: How to test the new devices in the market, expert recommendations[J]. J Visc Surg, 2023, 160(1): 52-54. doi: 10.1016/j.jviscsurg.2022.10.001
[9] GÖHLER D, OELSCHLÄGEL K, OUAISSI M, , et al. Comparative Analysis of Nebulizers in Clinical use for Pressurized Intraperitoneal Aerosol Chemotherapy (PIPAC)[EB/OL]. Medrxiv , [2023-06-21]. https://www.medrxiv.org/content/10.1101/2023.03.24.23287646v3.
[10] SOLAß W, HETZEL A, NADIRADZE G, et al. Description of a novel approach for intraperitoneal drug delivery and the related device[J]. Surg Endosc, 2012, 26(7): 1849-1855. doi: 10.1007/s00464-012-2148-0
[11] SOLASS W, KERB R, MÜRDTER T, , et al. Intraperitoneal chemotherapy of peritoneal carcinomatosis using pressurized aerosol as an alternative to liquid solution: first evidence for efficacy[J]. Ann Surg Oncol, 2014, 21(2): 553-559.
[12] ALYAMI M, HÜBNER M, GRASS F, et al. Pressurised intraperitoneal aerosol chemotherapy: rationale, evidence, and potential indications[J]. Lancet Oncol, 2019, 20(7): e368-e377. doi: 10.1016/S1470-2045(19)30318-3
[13] SOMASHEKHAR S P, ASHWIN K R, RAUTHAN A, et al. Pressurized IntraPeritoneal Aerosol Chemotherapy vs. intravenous chemotherapy for unresectable peritoneal metastases secondary to platinum resistant ovarian cancer – study protocol for a randomized control trial[J]. Pleura and Peritoneum, 2019, 4(1): 20180111. doi: 10.1515/pp-2018-0111
[14] CASELLA F, BENCIVENGA M, ROSATI R, et al. Pressurized intraperitoneal aerosol chemotherapy (PIPAC) in multimodal therapy for patients with oligometastatic peritoneal gastric cancer: a randomized multicenter phase Ⅲ trial PIPAC VEROne[J]. Pleura and Peritoneum, 2022, 7(3): 135-141. doi: 10.1515/pp-2022-0111
[15] SGARBURA O, VILLENEUVE L, ALYAMI M, et al. Current practice of pressurized intraperitoneal aerosol chemotherapy (PIPAC): still standardized or on the verge of diversification?[J]. Eur J Surg Oncol, 2021, 47(1): 149-156. doi: 10.1016/j.ejso.2020.08.020
[16] SGARBURA O, EVENO C, ALYAMI M, et al. Consensus statement for treatment protocols in pressurized intraperitoneal aerosol chemotherapy (PIPAC)[J]. Pleura Peritoneum, 2022, 7(1): 1-7. doi: 10.1515/pp-2022-0102
[17] NADIRADZE G, HORVATH P, SAUTKIN Y, et al. Overcoming drug resistance by taking advantage of physical principles: pressurized intraperitoneal aerosol chemotherapy (PIPAC)[J]. Cancers (Basel), 2020, 12(1): 34.
[18] RAMOS ARIAS G, SINDAYIGAYA R, OUAISSI M, et al. Safety and feasibility of high-pressure/high-dose pressurized intraperitoneal aerosol chemotherapy (HP/HD-PIPAC) for primary and metastatic peritoneal surface malignancies[J]. Ann Surg Oncol, 2023, 30(4): 2497-2505. doi: 10.1245/s10434-022-12698-4
[19] BAGGALEY A E, LAFAURIE G B R C, TATE S J, et al. Pressurized intraperitoneal aerosol chemotherapy (PIPAC): updated systematic review using the IDEAL framework[J]. Br J Surg, 2022, 110(1): 10-18. doi: 10.1093/bjs/znac284
[20] BUGGISCH J R, GÖHLER D, SOBILO J, et al. Development and technical validation of an ultrasound nebulizer to deliver intraperitoneal pressurized aerosols in a rat colon cancer peritoneal metastases model[J]. BMC Cancer, 2022, 22(1): 570. doi: 10.1186/s12885-022-09668-0
[21] 曹洪涛, 王腾飞, 吴勇, 等. 腹腔加压气溶胶化疗治疗结直肠癌腹膜转移研究进展[J]. 中国肿瘤临床, 2023, 50(14): 740-745.



 下载:
下载: